�}�������a
acute leukemia |
| �y�T�O�z | ������Y�ꂽ�ُ�N���[���̎�ᇐ����B�ˍ������̔����a�苅���L�j�זE�S�̂�30�� |
| �y���ށz | - �}�������������a�iAML�j
- MPO���F�ʼn苅��3���������BAuer���́i�{�j�̏ꍇ������
M0
�������^�����苅�������a | �ł���������AML�ŁAMPO�z���苅��3��
�d��or�Ɖu�w�I�����ɂč����n�̒���i�{�jand�����p�n�̒���i�|�j |
M1
�����苅�������a | �قƂ�Ǖ����X���������Ȃ����AM0���͕������Ă��� |
M2
�����^�����������a | �����X����AML�ŁA�c��苅��10���ȏオ�O�������ȍ~�ɕ������Ă���
������Auer���́i�{�j |
M3�iAPL�j
�O�����������a | 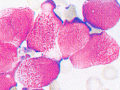 MPO�z���苅��100�� MPO�z���苅��100��
�O�������̌`�Ԃ������������a�זE�����B�i�j���Auer�����Afaggot�זE��F�߂�j
t�i15�G17�j�iq22�Gq21�j�̑��ݓ]�����݂��A�\��s�� |
M4�iAMMoL�j
�����P���������a | �������n�ƒP���n�̑o���ւ̕����X�������������a�זE�����B�A������Auer���́i�{�j
�G�X�e���[�[���F�ɂāA�������n�זE�̓N�����A�Z�e�[�gE�ɐ��܂�A�P���n�זE�̓u�`���A�Z�e�[�gE�ɐ��܂�i�P���n�͂����NaF�}�������z���j |
M5�iAMoL�j
�P���������a | �P���n�̐��i�����������a�זE�����B�A������Auer���́i�{�j
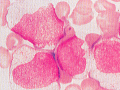 �G�X�e���[�[���F�ɂāA�u�`���A�Z�e�[�gE�ɂ̂ݐ��܂�ANaF�}�������i�{�j �G�X�e���[�[���F�ɂāA�u�`���A�Z�e�[�gE�ɂ̂ݐ��܂�ANaF�}�������i�{�j�EM5a�c���B�̒��S���c��ȒP�苅�BMPO�z���苅��3��
�EM5b�c���B�̒��S����r�I���n�����זE�ŁA�j�ɂ͒P���l�̐ꍞ�� |
M6
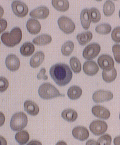
�Ԕ����a | �ԉ苅�n�ُ̈�N���[���i�Ԕ����a�זE�j�ƁA�����苅�����B
�i�Ԕ����a�זE���������̉苅��50���ȏ�A�����苅��30���ȏ�j
�Ԕ����a�זE�́A�j�����n�ŋ��ԉ苅�l�A���܂��܂Ȋ�`���APAS���F�ŋ��z�� |
M7
���ԉ苅�������a | ���j���̐��������������a�זE�����B�������̂ŁAMPO�z���苅��3��
�d��or�Ɖu�w�I�����ɂċ��j���n�̒���i�{�j
Down�ǂƊ֘A���[�����A30���ȏ�ɍ������ۏǂ̍������݂��� |
- �}�������p�������a�iALL�j
- MPO���F�ʼn苅��3���������BAuer���́i�|�j
| L1 | ���`�Ŋj���̂̂͂����肵�Ȃ������p�苅�l�̔����a�זE�����B�B������ALL�œ��ɑ��� | 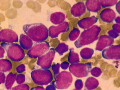 |
| L2 | ��r�I��^�Ŋj���̂̂͂����肵�������a�זE�����B
���l��ALL�ɂ悭�݂��� |
L3
�iBurkitt�^�j | �\�ʂɖƉu�O���u������F�߂�ABurkitt�����p��ɍ���������^�̍זE�����B�B����80����t�i8�G14�j�̐��F�ُ̈��L���� |
ALL��80���߂��͕���������B�זE�����a�ŁAcommon ALL�Ƃ���
|
| �y�u�w�z | �D���N��͏����i����2�`4�j�ƒ����N��w�B�O�҂ł�ALL�����S�A��҂ł�AML�̕������� |
| �y�����z | ���F�̂̓ˑR�ψق������ŁA�s���ȓ_�������BAML�ɑ����������a�̌����Ƃ��ẮA���w�Ö@�i�A���L�����܁A�G�I�g�|�V�h�Ȃǂ̃g�|�C�\�����[�[�j�Q��j�A���ː��Ǝ˂Ȃǂ�����BALL�̈ꕔ�ł�Ph1���F�̂����o����� |
| �y�Ǐ�z | �����}���ɂ��Ǐ�c�n���Ǐ�i�����A����A���ӊ�etc.�j�A�Պ������A�o���X���i�畆�̓_��o���A�S���o��etc.�j
����Z���ɂ��Ǐ�c���B��A�����p�ߎ�i����ALL�j�A���ɁA�ߒɁA�������i���ɏ�����ALL�ɑ����j�AAML�ł͗ΐF��E�ዅ�ˏo�AM4�EM5�ł͎�����E�����o��
���̑��cM3�ł�DIC |
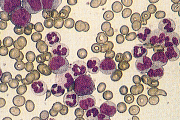
| �y�����z | ��������WBC�����A�c��苅�i�{�j�A�����a��E�i�{�j�ARBC���AHb���AHt���APlt���ANAP���`�� �����ˈ�ʂɉߌ`���A�����a�苅����́i���L�j�זE�S�̂�30���j �����w�ˌ���LDH���A�����A�_���AM4�EM5�ł͌����E�A�����]�`�[�����AALL�ł�TdT�����i�{�j |
| �y�\��z | ���l��AML�c60�`80���Ŋ��S�����A5����15��
������ALL�c90�������S�����A5����60���ȏ�i�\��s�Lj��q�c1�Έȉ�or10�Έȏ�A�j���AWBC��2���ABurkitt�^�AT�EB�זE�\�ʃ}�[�J�[�i�{�j�A�c�u��ᎁA�����_�o�Z���APh1���F�́i�{�jetc.�j |
| �y���Áz | ���w�Ö@�c�����Ö@���n�łߗÖ@�������Ö@���ێ��Ö@
�E�����Ö@�FAML�ł̓_�E�m���r�V���iDNR�j�E�V�^���r���iAra-C�j���S�B�������AM3�ł�ATRA��
ALL�ł�L-�A�X�p���M�i�[�[�iASP�j�E�r���N���X�`���iVCR�j�E�v���h�j�]�����iPSL�j��ATRA�i���`�m�C���_�j�̕���p�cATRA�nj�Q�i�x�Z������O2���ǁj�A�畆�E�S���̏�Q�A��������etc. �E�n�łߗÖ@�F��������̋��͉��w�Ö@
�E�����Ö@�F�Ԍ��I�ȋ��͉��w�Ö@
�E�ێ��Ö@�F�����I�ȓŐ��̒Ⴂ���w�Ö@
�����ڐA�c50�Έȉ��A���w�Ö@�ɂ�鎡��������ȃP�[�X���K���̒��S
�x���Ö@�c�K�v�ɉ����āA�Ԍ����A���A�����A���A�R���ܓ��^�A�A�t�A�A���v���m�[�����^etc. |
|
| hairy cell leukemia |
| �y�T�O�z | �`���זE�̑O�i�K��B�זE�R���̔����a | 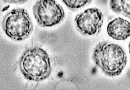 |
| �y�u�w�z | ���N�ȍ~�̒j���ɍD�� |
| �y�Ǐ�z | �ɏ��i�s���ŁA�����B��Ȃǂ������� |
| �y�����z | �Č��������A��Ύ_��R���_�z�X�t�@�^�[�[�i�{�j�A����dry tap�A�є���ˋN��L���锒���a�זE |
| �y���Áz | IFN���A�f�I�L�V�R���z�}�C�V�� |
|
�����ٌ`���nj�Q
myelodysplastic
syndrome�iMDS�j |
| �y�T�O�z | �������זE�ɐ������ُ�N���[���̑��B�˖��������ɂ��Č��������ior��n���̌��������j |
| �y�u�w�z | ������ɍD���B�����ɋ}�������a�Ɉڍs�i�O�����a����j |
| �y���ށz |
| �a�^ | ��������
�苅 | ������
�苅 | �����a�ւ�
�ڍs | ���̑��̓��� |
| �s�����n���iRA�j | ��1�� | ��5�� | low risk�Q | �@ |
��S�苅��RA
�iRARS�j | �������̊�S�苅��15���A�S�苅���n���̈ꕔ���\�� |
| �苅������RA�iRAEB�j | ��5�� | 5�`20�� | high risk�Q | �@ |
| �ڍs����RAEB�iRAEB-t�j | ��5�� | 20�`30�� | RAEB���}�������a�Ɉڍs������i�K�BAuer���́i�{�j�BWBC�� |
���������P���������a
�iCMMoL�j | ��5�� | ��20�� | ���������P�����AWBC���A�������]�`�[���� |
|
| �y�Ǐ�z | �n���Ǐ�i�����A����A���ӊ�etc.�j�A�Պ������A�o���X���i�畆�̓_��o���A�S���o��etc.�j |
| �y�����z | ���������Č��������iRBC���AHb���AHt�����AWBC��or���APlt���j�A�苅�i�{�j�A�����̌`�Ԉُ�i�D�������UPelger-Hue�Nt�j�ُ��A���匌�����j�ANAP��or�� �������Α勅�����F�f���n���ƂȂ� �������ߌ`���A�苅��30���A�������� ���̑��c50�`70�������F�ُ̈� | 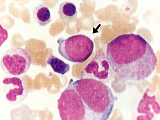 |
| �y���Áz | low risk�Q���o�ߊώ@�����S�B�K�v�ɉ����Ďx���Ö@�i�Ԍ����A���A�����A���A�R���܁EG-CSF�̓��^�j high risk�Q�ˎx���Ö@�ɉ����āA�����ڐA�AAML�ɏ��������͉��w�Ö@�A����Ara-C���^etc. |
|
���������������a
chronic
myelocytic
leukemia�iCML�j |
| �y�T�O�z | ���\�����זE����ᇐ����B |
�@
 |
| �y�����z | �t�B���f���t�B�A���F�́iPh1���F�́j��t�i9�G22�j�iq34�Gq11�j�̑��ݓ]���Abcr/abl�̃L������`�q�̍��o���`��������Tk������L���� |
| �y�u�w�z | �����N��w�ɑ������A�p�x��AML�̖�1/4 |
| �y�Ǐ�z | �ɏ��i�s���ŁA���o�Ǐ�����܂蔺�킸�A���R���������P�[�X���قƂ�ǁB�i�s����A�����B���A�̎��A�H�~�s�U�������� |
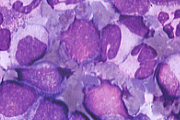
| �y�����z | �������������a��E�i�|�j�AWBC�����i�c��苅�����n�������j�A
Neutro.���AEosino.���ABaso.���ANAP�����ARBC���AHb���APlt���i��Ɂ��j �������ߌ`���iM/E�䁪�j�A���j���� �����w������Vit. B12���A�s�O�aVit. B12�����\���A�����A�_���A����LDH���A�����q�X�^�~���l�� |
| �y�\��z | �����ڐA���s��Ȃ�����A�f�f�m��㕽��3�`4�N���}���]�����N�����Ď��S���� ���}���]���������Ɩ��������苅�䗦��30���A�}�������a�ɗގ�����a��i�}�������a�l�̗Տ��Ǐ�A�����a��E�i�{�j�ANAP��etc.�j��悷��B�����͓��������ۏǂƂȂ�Adry tap������ |
| �y���Áz | �������̎��� �����ڐA�c50�Έȉ��AHLA��h�i�[�̓�����P�[�X��first choice
IFN-���Ö@�c�����ڐA�̓K�����Ȃ��Ǘ�ɑ���first choice�B�����P�[�X�ƌ����Ȃ��P�[�X�̍����������A����p������ ���ŋ߂ł�IFN-����������p�̏��Ȃ��C�}�`�j�u����1�I���ɂȂ����
�q�h���L�V�E���A�c�Տ��Ǐ���P�̈Ӗ������Ȃ��A�}���]���̗\�h�͂ł��Ȃ� �}���]�����̉��w�Ö@���r���N���X�`���iVCR�j�{�v���h�j�]�����iPSL�j�̕��p�Ö@ |
|
���������p�������a
chronic
lymphocytic
leukemia�iCLL�j |
| �y�T�O�z | �ُ�N���[�������������`�̃����p���i95����B�זE�n�j�������𒆐S�Ɏ�ᇐ��ɑ��B�ˉt���Ɖu�s�S�i�זE���Ɖu�s�S�������j |
| �y�u�w�z | ���Ăł͕p�x�������S�����a�̖�30�����߂邪�A�킪���ł͖�3���Ŕ�r�I�܂�B�D���N���60�Α� |
| �y�Ǐ�z | ��댯�x�Q�i�p�x�������j�c�قƂ�ǖ��Ǐ�ŁA�����p�ߎ�A���B��݂���̂�
���댯�x�Q�c���M�A�̏d�����A�H�~�s�U�A�����p�ߎ�A���B��A�t���Ɖu�s�S�̈Պ����X���A���ȖƉu�����E������ᇂ̍��� |
| �y�����z | ��������RBC���AHb���AHt���AWBC�����APlt���ANAP�� �����ˏ��^�����p���̒��� ���̑��c������-�O���u�������A�c���i�|�j�APHA�����i�|�j�A����Coombs�����i�{�j�A����Vit. B12�� | 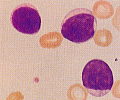 |
| �y���Áz | ��댯�x�Q�ˌo�ߊώ@�̂�
���댯�x�Q�˃V�N���z�X�t�@�~�h�̓��^etc. |
|
���lT�זE�����a
adult T-cell
leukemia�iATL�j |
| �y�T�O�z | HTLV-1������A20�N�ȏ���o�āAT�זE�n�̔����a/�����p��� | 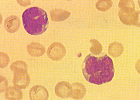 |
| �y�����z | HTLV-1�̐���/���s��/���t�����i�����������j |
| �y�u�w�z | �킪���ɖ�120���l�̃L�����A�����݂��A���̔����߂�������n��ɕ݂��Ă���B�L�����A���{�ǂ�����m���͔N��0.05�� |
| �y���ށz | �����Ԃ�^�i�����p����4000�A���Ǐ�j�A�����^�i�����p����4000�A���Ǐ�j�A�����p��^�i�����p�ߎ����j�A�}���^�i���܂��܂ȗՏ��Ǐ��悵�ċ}���ɐi�s�j |
| �y�Ǐ�z | �����p�ߎ��A���B��A�畆�Z���i�g���A�牺���߁A�u�]etc.�j�A������Ǐ�i���S���Z���A��Ca���ǁj
�����ǁc�����x�����A��������AM�`�����ǁA�����t�s�S�A�����畆�^�ۏ�etc. |
| �y�����z | ��������WBC�����A�ԕُ�̎�ᇍזEflower cell ���̑��c�����RHTLV-1�R�́i�{�j�A����Ca���A����LDH���A�c���i�|�j |
| �y���Áz | �����Ԃ�^�E�����^�˖����ÂŌo�ߊώ@
�����p��^�E�}���^��non Hodgkin�����p��ɏ��������Ö@���s���邪�A�\��͒������s�� |
|
�������ۏ�
myelofibrosis
�iMF�j |
| �y�T�O�z | �ُ�N���[�����������������זE����ᇐ����B�ˑS�g�̍����g�D�̐��ۉ��A���O�����Ƃ���ɔ��������B���A���ԉ苅�� | 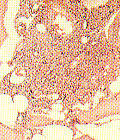 |
| �y���ށz | �������������ۏǁc60�ΑO��ɍD��
�������������ۏǁc������ᇂ̍����]���A�����a�A������A���������p��A���j�A�x���[�����łȂǂɂ�� |
| �y�Ǐ�z | �ɏ��i�s���ŁA�n���Ǐ���B����S�Ǐ�B���̑��A�E�G�]���ɁA�̎��A�喬�����i�Ǐ�etc. |
| �y�����z | �����������������F�f���n���A���ԉ苅�����AWBC���ANAP���APlt���A�����̌`�Ԉُ�i�ܓH�Ԍ����A���匌����etc.�j
�����ԉ苅�ǁileukoerythroblastosis�j�c���������ɒʏ�͔F�߂��Ȃ��c���������n�זE�Ɛԉ苅�������ɏo�������ԁB�������ۏǂ̑��A������ᇂ̍����]���Ȃǂł݂��� �����ː��ۉ��idry tap�j�A��`���A���j�����A���g�D�̍d���A������� �����w�ˌ���LDH���A�����A�_���A����I-Bil���AALP���A�������]�`�[�����A����Vit. B12�� |
| �y�\��z | ���ϐ������Ԃ�4�`5�N�ŁA�����Əo���X������v�Ȏ����B�܂��A�o�ߒ��ɋ}�������a�l�̓]�������������Ƃ����� |
| �y���Áz | ���ٓI�Ȏ��Ö@�Ȃ� |
|
| �ޔ����a���� |
| �y�T�O�z | ���炩�̊�b�����ɑ��Č��t�n�������������ʁA�����a�ɗގ����錌�t������悷��Ɏ��������� |
| �y�����z | ��b�����Ƃ��āA������ᇂ̍����]�ځA�����ǁi�������j�A�`�����P�j�ǁA�S���Petc.�j�A���������ǂ̉��A�}���ȗn�������̉��A��o���̒���etc. |
| �y�����z | ��������WBC����or�c��苅�̏o���ANAP�� |
|
| ���������� |
| �y�T�O�z | �D��������200�`300/��l |
| �y�����z | �Տ���͖�܂ɂ����̂��d�v �E�A�~�m�s�����Ȃǂ��s�����n��M���ł́A�U�^�A�����M�[�ɂ�錌���j�N����
�E�N�����v���}�W���Ȃǂ̃t�F�m�`�A�W���U���́A���`�}�]�[���E�v���s���`�I�E���V���Ȃǂ��R�b��B���A�R������ł���`�N���s�W���Ȃǂł��݂���i��A�����M�\���j |
| �y�Ǐ�z | �A�����M�\���˓��^�㐔���ɁA�����A���M�A���s���������A�G�����A�L�ɐ������p�ߎ�Ȃǂ̏Ǐo��
��A�����M�\���˓��^�㐔�T�ԂɁA���M���̊����Ǐo���B�s���ǂɎ��邱�Ƃ����� |
| �y�����z | ��������WBC���ANeutro.�����ALymph.�� �����˒�`���`�ߌ`���A���ɂ͗ޔ����a�������݂��� |
| �y���Áz | ������܂̒��~�A�����Ǒ�i�����\�h�A�R���������^�AG-CSF���^�j�A�X�e���C�h�̓��^
���������A���͋֊��iGVHD�̊댯������j |
|
�`�����P�j��
infectious
mononucleosis
�iIM�j |
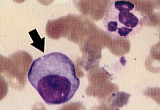
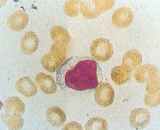
| �y�T�O�z | EBV��B�זE�ɑI��I�Ɋ�����B�זE�̕s������CTL���������˖Ɖu�����ɂ�鉊�ǔ��� |
| �y�����z | ��N���l�ȍ~��EBV�ւ̏������������BCMV�AHBV�AHCV�A���]�E�C���X�ȂǑ����̃E�C���X�ł��{�ǂɗގ��̏Ǐ�����������Ƃ�����i�`�����P�j�Ǐnj�Q�j |
| �y�Ǐ�z | ���T�Ԃ̐������̌�A���M�A�����ɁA�����p�ߎ�A�G�����ԁi�����Δ����U�����`���j�A���B��A���]etc. |
| �y�����z | ��������WBC���ALympho.�����iCD8�z����CTL�ATs�������j�A�ٌ^�����p�� �����w��AST���AALT���AALP�� �E�C���X�R�̉�
| IgM�^VCA�R�� | �������`�}�����i�����IgG�^�ɒu�������j |
| IgG�^VCA�R�� | �}�����`���i�I���A�h��R�̂ƂȂ�j |
| IgG�^EA�R�� | �}�����`���i������������IgG�^���o���j |
| IgG�^EBNA�R�� | ���i��NA��nuclear antigen�̗��j |
|  |
| �y���Áz | �\��͗ǍD�ŁA���T�ԂŎ������� ���y�j�V�����n�͋֊� |
|
���������p��
malignant
lymphoma |
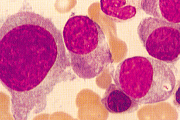
| �y�T�O�z | �����p�n�זE����ᇐ����B�������p�g�D�i�����p�߁E�Betc.�j | 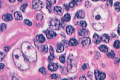 |
| �y���ށz | - Hodgkin�a�iHD�j
�����p�g�D�����ɂāAReed-Sternberg�iRS�j�זE�i�j��������悷��A����Ȋj���̂�L���鑽�j�̋��זE�j
Rye���ށi�g�D�w�I���ށj
| �����p���D�ʌ^�iLP�^�j | �ُ푝�B���Ă��郊���p���̒��ɁA������RS�זE���݂��� |
| ���ߍd���^�iNS�^�j | ���ߏ�ɑ��˂�ꂽ���B�����p���̒��ɁARS�זE���U�� |
| �����זE�^�iMC�^�j | �����p�������łȂ��AM�ӁE�`���זE�E�D�_���Ȃǂ�RS�זE�����͂ށB����ɐ��ۉ�������F�߂��� |
| �����p�����@�^�iLD�^�j | �����p�����������A�����Đ��ې��g�D�̑��B�������^�C�v�BRS�זE�͑����X���ɂ��� |
Ann Arbor���ށi�a������Cs�j
| Cs�T | 1�̃����p�ߗ̈� or 1�̐ߊO���ʂւ̐N�P |
| Cs�U | ���u���̏㉺�̂����ꂩ����ŁA�����̃����p�ߗ̈� or 1�ȏ�̃����p�ߗ̈�{�ߊO���ʂւ̐N�P |
| Cs�V | ���u���̏㉺�ɋy�ԕ����̃����p�ߗ̈�ւ̐N�P�B���邢�͂����1�̐ߊO���ʂւ̌��ǓI�N�P and/or �B�ւ̐N�P |
| Cs�W | 1�ȏ�̐ߊO���ʂւ̂т܂N�P |
|
| 6�����ȓ��ɂ�����10���ȏ�̑̏d�����A38���ȏ�̔��M�A�����������B�Ƃ���B����炪�Ȃ����A�Ƃ��� |
- ��Hodgkin�����p��iNHL�j
- �P�N���[�����̎�ᇐ����B�Ɋ�Â������B�\�ʃ}�[�J�[�ɂ��A��ɏc�u���ɔ�������T�זE�^�Ǝ�ɕ����ɔ�������B�זE�^�ɕ�������
LSG���ށi�Z���x����̕��ށj
�h�E��
�����p�� | ��ᇍזE�����ߏ�ɑ��B���A�h�E���`���B�\��͊T���ėǍD
B�זE�ɗR�����A�قƂ�ǂ�t�i14�G18�j�iq32�Gq21�j�Ƃ������ݓ]���������Ă���
���זE�^�A�����^�A��זE�^�ɍו�������� |
�т܂�
�����p�� |  ��ᇍזE���т܂ɑ��B���Ă���^�C�v�B�킪���̈��������p��̑唼���߁A�\��͕s�� ��ᇍזE���т܂ɑ��B���Ă���^�C�v�B�킪���̈��������p��̑唼���߁A�\��͕s��
��ᇍזE�̋N����B�זE�n��T�זE�n�̗��������邪�AT�זE�n�̕�������ɗ\��s��
���זE�^�A���זE�^�A��זE�^�A���`�זE�^�A�����p�苅�^�ABurkitt�^�ɍו����������Burkitt�����p���c���A�t���J�̒j���ɍD�����邪�A�킪���ł͂܂�BB�זE�R���ŁA�����Δ���������BEBV�Ƃ̊֘A�Ac-MYC��`�q�ُ̈�Ƃ̊֘A���F�߂��At�i8�G14�j�iq24�Gq32�j�At�i8�G22�j�iq24�Gq11�j�At�i2�G8�j�ip12�Gq24�j�Ƃ���3��ނ̑��ݓ]�����������Ă��� |
- ���̑��̈��������p��
�E�Ɖu�苅�������p�ߏǁiIBL�j�c�S�g�̃����p�߂ŁA�Ɖu�苅�i�P�N���[������B�זE�j�ƌ`���זE�i���N���[�����j����ᇐ����B�B�Ǐ�Ƃ��Ă͔��M�A�̏d�����A�����A��]�i�u�]���g���������j�Ȃǂ��݂���B���ȖƉu�������̍����������ACoombs�e�X�g�ŗz���������ꍇ������ �E�ۏ����c�畆�Ǐ�𒆐S�Ƃ���T�זE�n�����p��̈�� �ESe�Lzary�nj�Q�c�ۏ��ǂ��������������́B�ۏ��ǂ�Se�Lzary�nj�Q�����킹���畆T�זE�n�����p��iCTCL�j�Ƃ�����
|
| �y�u�w�z | compromised host�ɍD��
Hodgkin�a�ˉ��Ăł͑������A�킪���ł͐����B���ǔN��̃s�[�N��30�ΑO���60�Έȍ~
��Hodgkin�����p��˂킪���ł�90���ȏ���߂� |
| �y�Ǐ�z | - Hodgkin�a
- �����p�ߎ�c�����p�߂ɏ�������ꍇ�������A�A�����ɐi�W�B�ŏI�I�Ɋ��B���
�S�g�Ǐ�c�Ԍ��M�i�T�^�I�ɂ�Pel-Ebstein�^�j�A�����A�̏d�����A�~�y���A�����ǁi�я��v�]etc.�j�̍���etc.
- ��Hodgkin�����p��
- �����p�ߊO�g�D�i���W�G���A������etc.�j�ɏ����A��A�����ɐi�W�B�S�g�Ǐ�͂܂�ł��邪�A�����Δ��������݂��A�\���Hodgkin�a�ɔ�ׂĕs�ǁBBurkitt�����p��̏ꍇ�A�c���ɂ�����{�����ӂ̎�ᎁA�N�����ɂ����镠����ᎁi���̏ꍇ�A���d�ϏǂŔ��ǂ��邱�Ƃ�����j�������Ǐ�Ƃ��đ���
|
| �y�����z | �����������������F�f���n���AWBC���`���ALymph.���i��ΓI�����p�������ǁj�ANeutro.���AEosino.�� �����w��ESR���ACRP���A����LDH���A�n���C���^�[���C�L��2��e�́isIL-2R�j���A����ALP���A����Ca���A���������A��-�O���u������ �Ɖu�w�I�������זE���Ɖu���i�c���i�|�j�APHA�������j�A�t���Ɖu�� �a������̂��߂̌����c99mTc-�R���C�h��p���������p�Ǒ��e�A67Ga-citrate��p������ᇃV���`�A���E�����̊e��摜�����A�������hor����etc. |
| �y���Áz | �T�E�UA����Hodgkin�a�˕��ː��Ǝˁi���u������ł̓}���g���ƎˁA���ł͋tY���^�Ǝˁj
�UB�E�V�E�W����Hodgkin�a�ˉ��w�Ö@�iABVD�Ö@etc.�j�����S
��Hodgkin�����p��ˉ��w�Ö@�iCHOP�Ö@etc.�j�����S |
| �y�\��z | Hodgkin�a�̗\��c�����p���D�ʌ^���ł��\�オ�悭�A�����p�����@�^���\��s�ǂł��� ��Hodgkin�����p��̗\��K����q�c�N��i60�Έȏ�͗\��s�ǁj�A����LDH�l�A�p�t�H�[�}���X�X�e�C�^�X�i2�ȏ�͗\��s�ǁj�A�ߊO�a�ς̐��i2�ȏ�͗\��s�ǁj�A�a�� |
|
M
�`
��
��
�� | ������
myeloma |
| �y�T�O�z | �����ɑ��݂���`���זE����ᇐ����B���P�N���[��������-�O���u�������ǁiM�`�����ǁj |
| �y���ށz | �Ɖu�O���u�����̎�ނɂ��AIgG������AIgA������AIgD������AIgE������ABence Jones�^���������ɕ������� ��Bence Jones�^�����56���Ŕ������A100���ōėn������Ƃ�������������Bence Jones�`���iBJP�j�݂̂��Y�����鍜����BBJP�̐��͉̂ߏ�ɐ��Y���ꂽL���ł��� ��ᇂ̑��B�l������A�Ǘ���������A������������A�т܂�����ɕ������A�������������̂͌`���זE�������a�Ƃ��� |
| �y�u�w�z | 70�Α�̍���҂ɍD���BIgG������S�̂̔����ȏ���߂� | |
| �y�Ǐ�z | ���a�ρc����w�����u���ŏ�������ꍇ�������B�Ғł̈������܂�a�I���܂��݂���
�ˍ��a�ς̌��ʁA��Ca���ǂƂȂ�A������Ǐ�A�ӎ���Q��
�n���Ǐ�c�����A����A���ӊ�etc.
�`���ُ�ɂ��Ǐ�c�Պ������ABence Jones�^������ł͋߈ʔA�Ǐ�Q�A�������A�~���C�h�[�V�X
�������p�n�a�ς͂߂����ɂ݂��Ȃ� |
| �y�����z | ��Xp��punched out lesion �������˒����x�̐��������F�f���n���A�A�K�`�� �����˒�`���X���A�ٌ^���̋����`���זE�A�j���͖��� �����w�˒P�N���[��������-�O���u�������ǁAM�`���AAlb���AESR�����A���t�̔S�f�x���A�Ìŏ�Q�ACa���A��2-MG�� ���̑��c�������A�~���C�h�[�V�X�A����Chol���A�t�s�S�̏��� |
| �y�\��z | �f�f��̕��ϐ������Ԃ͖�40���� |
| �y���Áz | ���w�Ö@�iMP�Ö@ or CP�Ö@�j�A���ː��ƎˁA�y�x�̒���I�ȉ^���Ö@�A�\���ȗA�t�A�Պ������ɑ����etc. |
|
�}�N���O���u����
����
macroglobulinemia |
| �y�T�O�z | �����p���l��IgM�Y���זE����ᇐ����B���P�N���[��������-�O���u�������ǁiM�`�����ǁj |  |
| �y�u�w�z | �����p�x�͍������1/10���x�B����҂ɑ��� |
| �y�Ǐ�z | �����p�n�a���c�����p�ߎ�A���B��etc.
�ߔS�f�x�nj�Q�c�_�o�Ǐ�i�߂܂��A���ɁA�z��etc.�j�A�S�s�S�A�Ìŏ�Q�A���ُ폊���i�Ԗ��Ö��̃\�[�Z�[�W�l�֍s�A�o����etc.�j
���̑��c�N���I�O���u�����ɔ���Raynaud�Ǐ�E�����@���]�A�Պ����X��etc. |
| �y�����z | �������˒����x�̐��������F�f���n���A�A�K�`�� �����˒�`���A�ُ�ȃ����p���l�̎�ᇍזE �`���ُ�c����-�O���u�������ǁAM�`���AIgM�����AIgG���AESR�����ASia water�����i�{�j |
| �y�\��z | ��������͗\��ǍD�ł��邪�A���ϐ������Ԃ�60�������x |
| �y���Áz | ���w�Ö@�i�V�N���z�X�t�@�~�hetc.�j�A�ߔS�f�x�nj�Q�ɑ������������A�X�e���C�h�̓��^etc. ���n���Ǐ�͖ڗ������A�A�����K�v�Ȃ��Ƃ͏��Ȃ�
�@ |
|
H���a
�i�d���a�j |
| �y�T�O�z | �Ɖu�O���u������H�����Y�����郊���p���l�̍זE����ᇐ����B |
| �y�u�w�z | ����߂Ē��������� |
| �y�Ǐ�z | ���������p��ɋ߂� |
|
monoclonal
gammopathy of
undetermined
significance
�iMGUS�j |
| �y�T�O�z | M�`����F�߂���̂́A������������̂悤�Ȓ�����������́B�ȑO��benign monoclonal gammopathy�Ƃ��Ă��� |
| �y�Ǐ�z | ���ɏǏ�͂Ȃ� |
| �y�����z | ���t�ˍ���-�O���u�������ǁAM�`���ȊO�̌����Ɖu�O���u�������AESR�� |
| �y���Áz | �o�ߊώ@��O.K. |
| �y�\��z | 10�`20���͑�����������Ɉڍs���� |
|
�����ÐH�nj�Q
hemophagocytic
syndrome |
| �y�����z | ���������p���iLAHS�Ƃ���j�A�E�C���X�������iVAHS�Ƃ���B����EB�E�C���X�������j�������B���ɂ́A�P���a�i����Still�a�ASLE�j�A������ᇁi�Ō`���A�}�������a�jetc. |
| �y�a�ԁz | ��L�̂悤�Ȍ����ˍ��T�C�g�J�C�����ǁ�M�ӂُ̈튈�����ˎ��Ȍ������ÐH |
| �y�Ǐ�z | �Č��������ɂ��Ǐ�i�n���A�Պ������A�o���X��etc.�j�A���t�A���B��A�����p�ߎetc. |
| �y�����z | ���t�����˔Č��������ALDH���A�t�F���`�������i�����������ꂽM�ӂ���Y�������j�AAST���AALT���ABil���A�n�v�g�O���r����etc. | 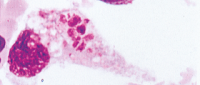 |
| �y�a���z | �����ÐH���i�������j |
| �y���Áz | �������̎��� |
| �y�\��z | ����LAHS�͗\��s�� |
|